Tekanan Pada Gas Ideal
tekanan gas ideal berlaku hukum boyle yang menyatakan baha pada jumlah mol dan sushu tetap, volume akan berbanding terbalik dengan tekanan gas. Persamaan tekanan gas ideal dirumuskan sebagai berikut
N = banyaknya partikel gas = 6,02 x 1023
m = massa dari 1 partikel gas (Kg)
v = kecepatan gerak partikel gas (m/s)
V = volume gas (m3)
P = tekanan gas ideal (N/m2)
oleh karena kita tahu bahwa energi kinetik dirumuskan Ek = ½ mv2 maka persamaan di atas dapat diubah menjadi
dengan Ek = Energi kinetik gas (satuan joule).
Persamaan Gas Ideal
Dalam gas ideal berlaku 3 hukum tentang kinetika gas yaitu
Hukum Boyle : V ∝ 1/P (n dan T tetap)Hukum Charles : V ∝ T ( n dan P konstan)Hukum Avogadro V ∝ n ( P dan T tetap)
Dari ketiga hukum di atas, dapat dikatakan volume gas berbanding langsung terhadap jumlah gas dan suhu dan berbanding terbalik terhadap tekanan, dirumuskan persamaang gas ideal
atau
N = jumlah partikel gas
n = jumlah mol gas
R = tetapan gas umum 8,31 x 103M/mol K
k = tetapan Boltzman = 1,38 x 10-23 J/K
untuk menentukan jumlah mol gas (n) sobat dapat menggunakan 2 alternatif rumus berikut
atau
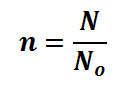
No = bilangan avogadro 6,02 x 1023
Mr = massa molekul relatif gas
m = masa partikel gas
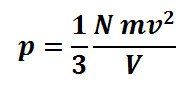

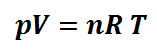
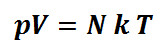

Tidak ada komentar:
Posting Komentar